اپیدمی چاقی سلامت عمومی را در جهان توسعه یافته به چالش می کشد و کیفیت زندگی را کاهش می دهد و سلامتی را تهدید می کند، حتی در شرایطی که نیاز به سرمایه گذاری های سنگین در مراقبت های پزشکی پیشگیرانه و درمانی دارد. کشف داروهایی که میتوانند مسیرهای روده-مغزی را تعدیل کنند، میتواند یک پیشرفت بالقوه در این زمینه باشد و به افراد چاق برای کاهش وزن و مبتلایان به دیابت کمک میکند تا متابولیک طبیعی خود را به دست آورند، حداقل و همچنین جراحی چاقی.
مقاله جدید در مجله تحقیقات بالینی داروهایی را توصیف می کند که می توانند به کاهش وزن و مدیریت دیابت نوع 2 (T2DM) کمک کنند.
 مطالعه: دو آگونیست گیرنده هورمون روده برای دیابت و چاقی. اعتبار تصویر: SHISANUPONG1986 / Shutterstock
مطالعه: دو آگونیست گیرنده هورمون روده برای دیابت و چاقی. اعتبار تصویر: SHISANUPONG1986 / Shutterstock
معرفی
علاوه بر کاهش خطر و شدت T2DM، کاهش توده بدن به میزان 5 تا 10 درصد مدتهاست که برای کاهش خطر چاقی شناخته شده است. بدیهی است که چاقی علت اصلی T2DM است.
متداول ترین روش ها برای دستیابی به این نتیجه مطلوب شامل تغییر رژیم غذایی و شیوه زندگی است. با این حال، آنها به اندازه کافی برای حفظ وزن مطلوب برای اکثر افراد کارآمد نیستند. در حالی که تعدادی از داروها برای درمان T2DM پدیدار شدهاند، برخی از آنها، از جمله انسولین، باعث افزایش وزن میشوند و اثر مطلوب آنها بر سلامت را تضاد میکنند.
تعدادی از قرص های کاهش وزن و سایر داروهای مبارزه کننده با چاقی متوسل شده اند، اما دارای عوارض جانبی بالقوه جدی هستند. جراحی چاقی با از دست دادن مقدار زیادی وزن در طول سال ها و بازیابی حساسیت به انسولین موثرتر است. با این حال، گران و پرخطر است و برای بسیاری از افراد ایده آل نیست.
تمرکز اخیر تحقیقات بر استفاده از هورمونهای روده برای کاهش ناهنجاریهای متابولیک زیربنایی T2DM و چاقی بوده است. هورمون های روده در ارتباط دو طرفه بین مغز و روده نقش دارند.
آگونیسم GLP1R
یکی از این مسیرها با واسطه پپتید روده مانند پپتید گلوکاگون 1 (GLP1) است که مشابههای آن در عمقی برای تأثیراتشان در این مناطق مورد مطالعه قرار گرفتهاند. GLP1 در روده کوچک تولید می شود و ترشح انسولین را بعد از غذا افزایش می دهد و در نتیجه سطح گلوکز خون را کاهش می دهد. با این حال، این پپتید به سرعت توسط یک آنزیم پروتئاز دی پپتیدیل پپتیداز IV غیرفعال و از بین می رود، که به این معنی است که کاربرد بالینی کمی دارد.
به زودی، یک آگونیست مصنوعی مقاوم به پروتئاز GLP1R، اگزناتید، بر اساس کشف خوش شانس یک فرم مقاوم به پروتئاز از پپتید GLP1R به نام اگزندین-4، در زهر هیولای گیلا ساخته شد. Exenatide برای درمان T2DM در سال 2005 تولید و تایید شد. پس از آن لیراگلوتاید، با نیمه عمر طولانی تر، برای درمان چاقی با دوز بالاتر در سال 2010 تایید شد.
سماگلوتاید یک آگونیست گیرنده GLP1 (GLP1R) است که برای استفاده در چاقی تایید شده است و باعث کاهش وزن 15 درصدی در آزمایشات بالینی و کاهش هیپرگلیسمی در بیماران T2DM می شود. در سال 2017 برای T2DM و در سال 2021 در چاقی مورد تایید قرار گرفت.
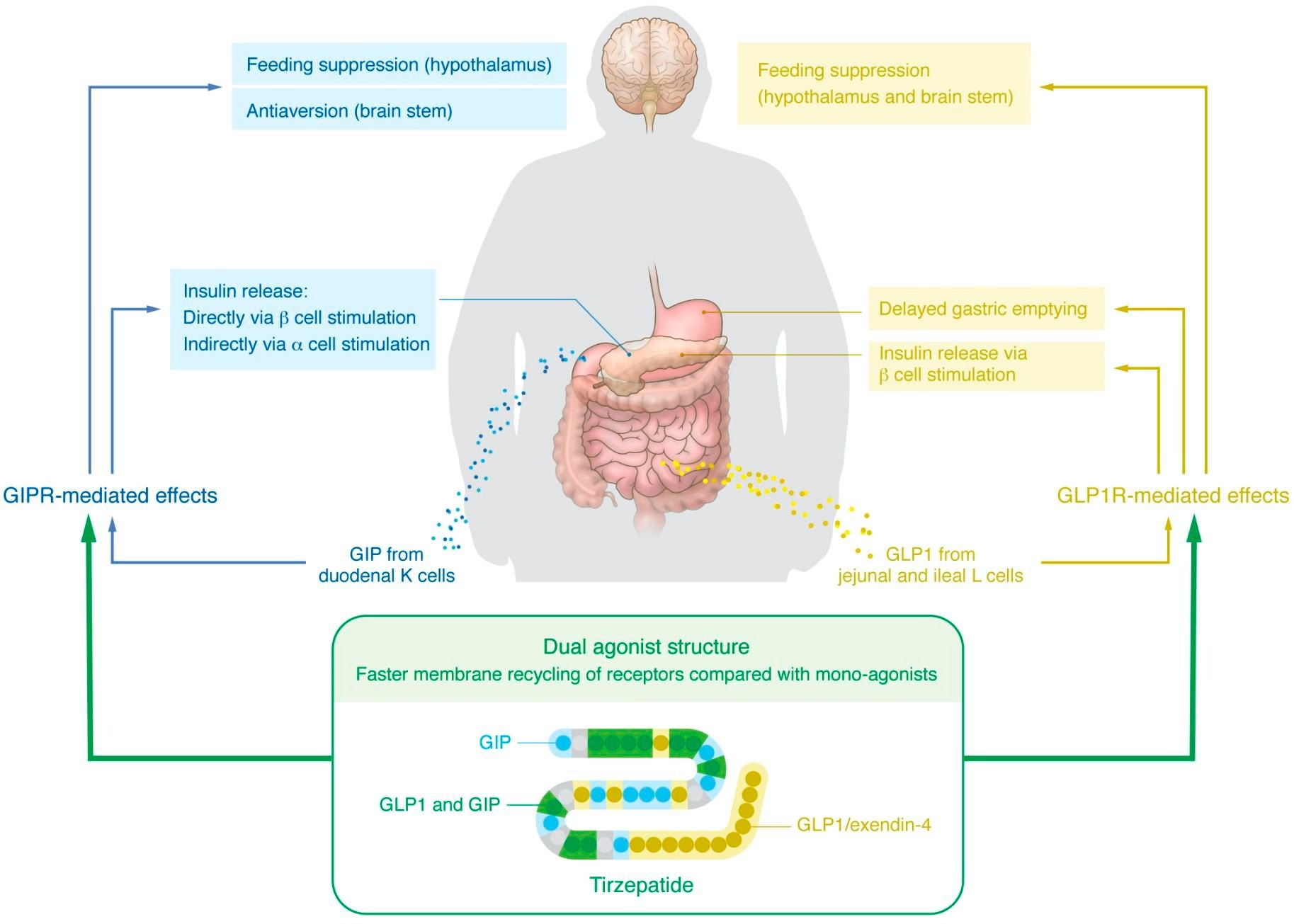 مکانیسمهای زیربنایی تنظیمکننده گلوکز و کاهش وزن هماگونیسم GIP/GLP1R را ایجاد و پیشنهاد کرد.
مکانیسمهای زیربنایی تنظیمکننده گلوکز و کاهش وزن هماگونیسم GIP/GLP1R را ایجاد و پیشنهاد کرد.
تیرزپاتید – یک درمان ترکیبی
اخیراً تیرزپاتید، آگونیست دوگانه گیرنده پلی پپتیدی بازدارنده معده/GLP1R (GIPR/GLP1R) به دنبال آن قرار گرفت. پپتید بازدارنده معده (GIP) تولید و آزادسازی انسولین را افزایش می دهد و آگونیست های GIPR در آزمایشات موش برای کاهش وزن بدن یافت شدند. بعداً، در سال 2013، یک آگونیست دوگانه مهندسی شده در GIPR/GLP1R سنتز شد و نشان داد که سطح گلوکز خون و وزن بدن را در حیوانات آزمایشگاهی کاهش می دهد.
با تثبیت ایمنی و اثربخشی چنین هم آگونیستهایی، تیرزپاتید اولین دارویی بود که در سال 2022 برای درمان T2DM تأیید شد. در بیماران چاق، این دارو باعث کاهش بیش از یک پنجم وزن بدن میشود.
اما چگونه به این اثر قابل توجه دست می یابد؟ تحقیقات در سطح مولکولی نشان میدهد که GIP روی GIPR سلولهای بتا پانکراس تأثیر میگذارد تا افزایش سطح انسولین پس از صرف غذا را افزایش دهد. در همین حال، GIPR روی سلول های آلفا پانکراس نیز با تحریک ترشح گلوکاگون باعث افزایش ترشح انسولین می شود. و در نهایت، GLP1R خود باعث افزایش ترشح انسولین می شود.
فعالیت مستقل در هر دو گیرنده ممکن است مسئول اثربخشی فوق العاده تیرزپاتید باشد. این موضوع هنوز محل بحث است، اما GIPR در مغز ممکن است مسئول کاهش وزن مرتبط با این دارو، به ویژه در مراکز هیپوتالاموس مرتبط با تغذیه باشد. قابل ذکر است، در دوزی که باعث کاهش وزن نمی شود، آگونیست GIPR می تواند کاهش وزن بدن مرتبط با آنالوگ GLP1 را افزایش دهد.
چندین مکانیسم در حال بررسی هستند، مانند بازیافت سریعتر GLP1R در داخل سلول با این هم آگونیست در مقایسه با آگونیست GLP1R خالص یا طیف گسترده تری از بیزاری از غذا خوردن ایجاد شده توسط آگونیست های GIPR. اگر مورد دوم درست باشد، این باعث افزایش فعالیت در GLP1R بدون اثرات نامطلوب روده مانند حالت تهوع که معمولاً با آگونیستهای GLP1R مرتبط است، خواهد بود.
در هر صورت، tirzepatide یک درمان ترکیبی برای T2DM و چاقی ارائه می دهد، امیدوارم اولین درمان از بین بسیاری از موارد باشد.
چشم انداز آینده
پلی آگونیست های بیشتری در حال توسعه هستند که ممکن است درمان پزشکی این شرایط سبک زندگی را متحول کنند و در عین حال از معایب مرتبط با جراحی چاقی اجتناب کنند. اینها شامل آنهایی هستند که به عنوان آگونیست در گیرنده های گلوکاگون/GLP1R عمل می کنند و هیپرگلیسمی ناشی از گلوکز را کاهش می دهند و در عین حال اثرات متابولیک مطلوب آن را حفظ می کنند. یکی از این موارد کوتادوتید است که وزن بدن و سطح گلوکز خون را از طریق GLP1R کاهش می دهد اما از بیماری کبد چرب غیر الکلی (NAFLD) از طریق فعال شدن گیرنده گلوکاگون جلوگیری می کند.
چنین ترکیباتی اثرات مطلوبی را در آزمایشات روی حیوانات و انسان نشان داده اند، با شواهدی مبنی بر کاهش وزن طولانی مدت در بیش از یک سال با یک دارو. اگرچه بیماران در این مرحله تنها به طور متوسط 5 درصد وزن بدن خود را از دست دادند، سایر اثرات گلوکاگون مانند لیپولیز و از دست دادن اشتها و همچنین چربی سوزی برای تولید گرمای بدن می تواند به بهبود تغییرات کبد چرب کمک کند. امروزه با افزایش تعداد بیماران سیروز مرتبط با NAFLD که نیاز به پیوند کبد دارند، این یک سوال داغ است.
Triagonists نیز در حال توسعه هستند که در هر سه گیرنده عمل می کنند تا تأثیر بیشتری بر ناهنجاری های متابولیک ایجاد کنند. اینها در حال حاضر در آزمایشات بالینی در حال آزمایش هستند.
چه پیامدهایی دارد؟
در حال حاضر، آگونیست های GLP1R، از جمله تیرزپاتید، باید از طریق تزریق، با دوزهای کوچک شروع شود تا عوارض جانبی نامطلوب، یا در برخی موارد، غیرقابل تحمل به حداقل برسد. فرمولاسیون های خوراکی برای برخی از داروها تولید می شود، اما از نظر اثربخشی ضعیف هستند.
نیاز مبرم به فرمولهای خوراکی قوی داروهای مولکولی کوچک است که میتوانند بهعنوان چند آگونیست و داروهایی با اثر آلوستریک در گیرندههای GIP، GLP1R و گلوکاگون عمل کنند. اینها باید کاهش وزن قابل توجه و بادوام را به همراه داشته باشند و نباید باعث افزایش مجدد وزن در هنگام توقف شوند. خطرات بالقوه آنها، از جمله سنگ کیسه صفرا، پانکراتیت و سرطان تیروئید، جدی است و باید به دقت مورد مطالعه قرار گیرد.
“گسترش سریع ابزارهای مولکولی برای کشف مکانیسم های اساسی زیربنای کنترل محور روده-مغز تغذیه و متابولیسم، همراه با تلاش برای مهار این مسیرها با نسل بعدی پلیگونیست های مهندسی شده، توسعه پزشکی دقیق برای چاقی، T2DM را بیشتر پیش خواهد برد. و بیماری های مرتبط“
مرجع مجله:
- باس، جی و همکاران. (2023). آگونیست های گیرنده هورمون های روده دوگانه برای دیابت و چاقی. مجله تحقیقات بالینی. آگونیست های گیرنده هورمون های روده دوگانه برای دیابت و چاقی. https://www.jci.org/articles/view/167952